CAS CLINIQUE
Un homme âgé de 74 ans était adressé en consultation par son oncologue pour un état douloureux évoluant depuis 4 mois. Il était suivi pour un adénocarcinome pulmonaire localisé (bilan d’extension par TEP scanner et IRM cérébrale négatif), en rémission complète après un traitement ayant comporté une lobectomie et 4 cures de chimiothérapie (carboplatine et paclitaxel) dont la dernière avait été réalisée 7 mois avant la consultation.
Dans les antécédents on retrouvait un tabagisme sevré 30 années auparavant, une hypercholestérolémie, une coronaropathie, un adénome de la prostate, une dilatation des bronches et un syndrome d’apnée du sommeil.
Chez la fille du patient, une spondyloarthrite HLA-B27 négative était suspectée, toutefois sans certitude du fait de la présence de pathologies rachidiennes mécaniques, ce qui faisait craindre ce diagnostic par le patient.
Les douleurs, apparues sans facteur déclenchant, étaient diffuses au rachis mais prédominaient au rachis lombaire. Elles étaient associées à des douleurs de la face externe des hanches. L’horaire de ces douleurs était mixte avec une prédominance mécanique. L’état général était conservé. A l’examen physique, le poids était de 90 Kg pour une taille de 178 cm. L’examen rhumatologique mettait en évidence une raideur lombaire globale
importante et une raideur cervicale modérée. L’examen des hanches et l’examen neurologique étaient normaux.
A l’interrogatoire, on ne retrouvait pas d’antécédent personnel ou familial de psoriasis, ni de symptôme pouvant évoquer une maladie inflammatoire colo-intestinale. La dernière biologie sanguine était sans anomalie particulière, et la CRP était mesurée à 2 mg/l.L’oncologue qui adressait le patient avait prescrit de l’ibuprofène à la posologie de 600 mg/jour, sans effet thérapeutique bénéfique. Il avait prescrit un scanner thoraco-abdomino-pelvien et une IRM du rachis lombaire. L’IRM lombaire ne montrait pas d’anomalie évocatrice de lésion tumorale. Il y avait des discopathies lombaires dégénératives peu sévères. Sur les séquences STIR, on observait un hypersignal triangulaire du coin antéro-inférieur de L3 siège d’une ossification vertébrale de type ostéophytique sur les coupes sagittales et un pont intervertébral latéral droit en L2-L3 de signal normal sur les coupes coronales (Figures 1a et 1b). Il existait également une image de type spondylite inflammatoire en L5.Sur les scanners TAP, le rachis thoraco-lombaire était visualisé en séquence osseuse. Il n’y avait pas d’ostéolyse de type tumoral. Il y avait de volumineuses ossifications prévertébrales et latérovertébrales droites, pontant 5 vertèbres thoraciques, dont le siège et l’épaisseur étaient évocateurs d’une hyperostose vertébrale engainante (HVE) (Figures 2a et 2b). Les coupes axiales passant par les articulations sacro-iliaques mettaient en évidence des ponts ostéophytiques en avant de la partie antérieure de l’interligne articulaire, sans érosion des berges osseuses et d’aspect compatible avec une HVE (Figure 3). Sur un autre plan de coupe, un début d’ankylose était visible à la partie antérieure de la sacro-iliaque droite.
Cette imagerie était évocatrice d’une HVE. Nous prescrivions une cure de naproxène (550 mg x 2/j) associé à de l’oméprazole. Revu en consultation7 semaines plus tard, le patient nous apprenait avoir arrêté rapidement le naproxène pour intolérance digestive.
Figures 1a et 1b. IRM du rachis lombaire en séquence STIR (coupes sagittale et coronale)
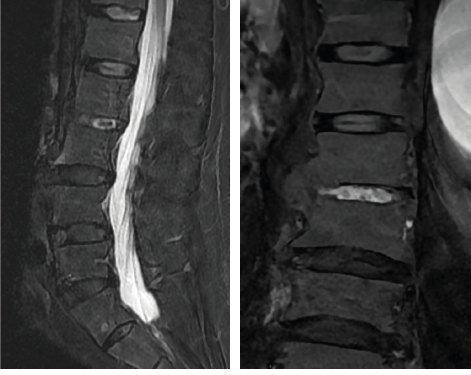
Figures 2a et 2b. Scanner osseux du rachis thoracique en coupes sagittale et coronale.
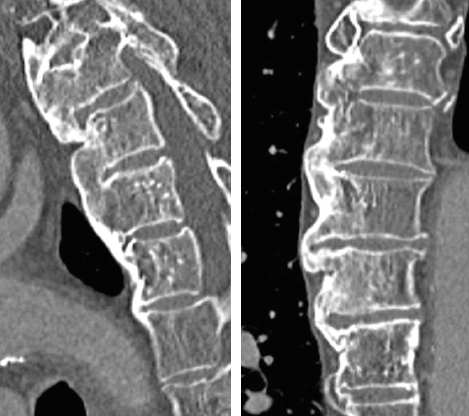
Figure 3. Scanner osseux des sacro-iliaques en coupe axiale.
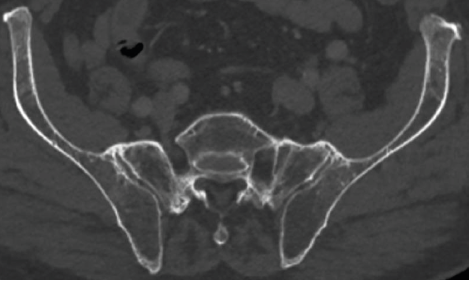
Les douleurs avaient d’ailleurs perdu de leur intensité mais persistaient. Nous prescrivions une cure de prednisone (30 mg/j), mais lors de la consultation réalisée 5 semaines plus tard, le patient déclarait ne pas avoir pu prendre la prednisone du fait des ruptures d’approvisionnement. Les douleurs avaient alors pris un caractère plus inflammatoire avec des lombalgies nocturnes. Un nouveau bilan biologique ne montrait pas de syndrome inflammatoire. Les phosphatases alcalines étaient très légèrement augmentées à 138 U/l. Les examens suivants étaient normaux : calcémie, gamma GT, électrophorèse des protides. Nous prescrivions de la prednisolone (20 mg/j) et de nouveaux examens d’imagerie : nouvelle IRM lombaire, radiographies et scintigraphie osseuses.
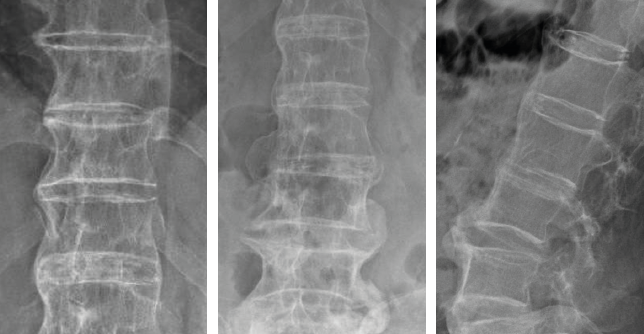
Revu quatre semaines plus tard, le patient déclarait avoir été amélioré de manière modérée par la prednisolone et ne prenait maintenant que du paracétamol à la demande. L’état douloureux persistait mais de manière à nouveau atténuée. Sur la nouvelle IRM lombaire, l’aspect était inchangé, notamment sans anomalie de type tumoral. Les radiographies de la charnière dorsolombaire et du rachis lombaire montraient de nombreux ponts vertébraux prédominant à droite, avec des aspects de pont ostéophytique hypertrophique mais aussi des ponts très peu épais de type syndesmophytique notamment en T12-L1 de face (Figures 4a, 4b et 4c). Les radiographies du rachis cervical objectivaient de volumineuses ossifications prévertébrales, très épaisses, aux étages C2-C3, C3-C4 et C5-C6, ainsi qu’une importante arthrose interapophysaire postérieure C4C5 bien visible de face (Figures 5a et 5b). Sur la scintigraphie osseuse au technétium 99m, il y avait de nombreuses hyperfixations siégeant uniquement à des sites d’ostéophytes et de ponts intervertébraux, au rachis lombaire des deux côtés et au rachis thoracique haut, surtout à droite (Figures 6a et 6b). L’ensemble des résultats et le recul permettait d’éliminer des lésions tumorales, de réfuter le diagnostic de spondyloarthrite et de confirmer la responsabilité de l’HVE dans cette poussée douloureuse axiale. Le patient était rassuré et nous prescrivions du paracétamol à la demande.
Figures 4a, 4b et 4c. Radiographies de la charnière dorsolombaire de face et du rachis lombaire de face et de profil.
Figures 5a et 5b. Radiographies du rachis cervical de profil et de face.
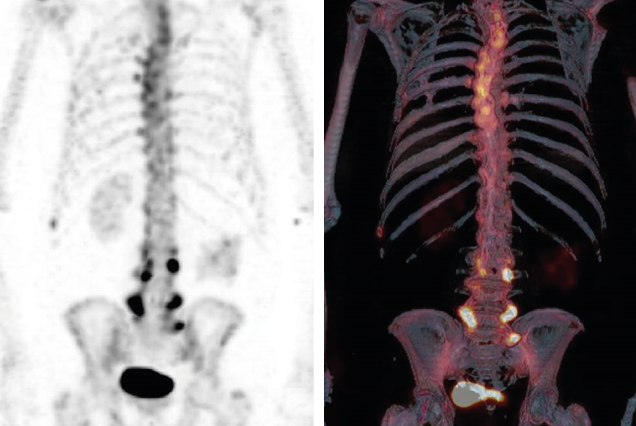
Figures 6a et 6b. Scintigraphie osseuse au technétium 99m.
DISCUSSION
L’hyperostose vertébrale engainante (HVE), encore appelée hyperostose vertébrale ankylosante, maladie de Forestier, ou Diffuse Idiopathic Skeletal Hyperostosis (DISH) dans la littérature anglaise, est une pathologie non inflammatoire de type dégénérative, caractérisée par une ossification des enthèses, prédominant au squelette axial mais pouvant atteindre les enthèses périphériques et dont le diagnostic est purement radiologique. Si elle a été décrite à la fin du XIXe siècle, les anomalies radiographiques et anatomopathologiques en ont été précisées par Forestier et Rotès-Querol en 1950 dans la revue Annals of Rheumatic Diseases1. L’étiologie de l’HVE, pathologie liée à l’âge et au sexe masculin, n’est pas connue. Si la plupart des sujets atteints d’HVE sont asymptomatiques et que la découverte de la pathologie est fortuite, certains patients présentent des symptômes dont la seule cause retrouvée est l’HVE, mais la fréquence des symptômes de l’HVE reste mal déterminée en dehors des complications compressives cervicales et du risque de fracture vertébrale pour des traumatismes à faible énergie.
Le diagnostic d’HVE repose sur l’aspect radiographique du rachis thoracique (rachis dorsal) où la maladie se traduit par des ossifications que l’on peut qualifier de vertébrales ou périvertébrales et qui se situent dans et autour du ligament longitudinal antérieur (ligament vertébral commun
antérieur)2,3. Il faut rappeler que ce ligament constitue une bande fibreuse descendant verticalement de la face externe de l’os occipital à la face antérieure de la 2e vertèbre sacrée, situé à la face antérieure des vertèbres et des disques intervertébraux (DIV). Il est épais et légèrement plus étroit sur les corps vertébraux et plus large au niveau des DIV. Ce ligament est attaché aux corps vertébraux dont il est en partie séparé par un tissu conjonctif à la partie moyenne et concave, tandis qu’il adhère plus qu’il ne s’attache aux DIV. Le ligament longitudinal antérieur est situé essentiellement à la partie antérieure de la colonne vertébrale, mais au rachis thoracique, de T4 à T12, il s’étend sur les parties latérales des corps vertébraux jusqu’aux articulations costo-vertébrales.
Les ossifications vertébrales au rachis thoracique sont au centre de toutes les classifications de l’HVE. Dans la classification proposée en 1976 par Resnick et Niwayama4, ces ossifications doivent former des ponts intervertébraux sur au moins 4 vertèbres contiguës (ceci sur des clichés de face ou de profil). De très nombreux systèmes de classification ont été proposés depuis, mais tous comportent pour principal item l’existence de ponts osseux vertébraux, généralement sur 3 ou 4 vertèbres thoraciques ou 4 vertèbres quelle que soit la localisation2. La classification diagnostique de Resnick et Niwayama précise que les ossifications forment des coulées le long des vertèbres pontées, et surtout que la hauteur des DIV correspondant est normale, contrairement aux ossifications visibles dans les discarthroses. Toutefois par la suite, le respect complet de la hauteur du DIV n’est plus formellement exigé car chez le sujet âgé, la coexistence avec des discopathies dégénératives est possible. De plus, la classification de Resnick et Niwayama exigeait des signes distinctifs par rapport à la spondylarthrite ankylosante : absence d’ankylose des articulations costo-vertébrales et interapophysaires postérieures, absence de sacro-iliite radiographique. Les classifications ultérieurement proposées n’exigent plus ces derniers éléments, mais font varier le nombre de vertèbres pontées, le caractère complet ou non des ponts (fusion ou non des extrémités), le siège des ponts vertébraux, l’épaisseur des ossifications et leur caractère en coulée2. Certaines font prendre en compte l’ossification possible des enthèses périphériques. Si aucune classification nouvelle ne fait l’objet d’un consensus, ce qu’il est important de comprendre c’est que la classification de Resnick et Niwayama, qui reste la plus utilisée, ne permet de diagnostiquer l’HVE qu’à un stade tardif (à l’instar de la classification de New York pour la SPA), ce qui empêche un diagnostic précoce et donc une analyse de l’évolution naturelle de la maladie. Néanmoins, il est démontré, notamment dans les études par scanner, que les ossifications progressent au fil du temps et donc que l’aspect radiologique ne peut qu’évoluer en aspect et en diffusion2.
La prévalence de l’HVE a été estimée dans différentes études de manière très variable, allant de 2,9 % à 42 %5. Dans une étude hollandaise publiée en 20086, dans une population de 501 patients âgés de 50 à 91 ans (moyenne 66,6 ans), la prévalence de l’HVE (critère de Resnick et Niwayama au rachis) est de 22,7 % chez l’homme et 12,1 % chez la femme (prévalence globale 17 %). Cette prévalence augmente avec l’âge : 11 % pour la tranche 50-59 ans, 17 % pour celle de 60-69 ans, 22 % pour celle de 70 ans et plus. Dans une étude réalisée aux USA et publiée en 2011, la prévalence de l’HVE (critère de Resnick et Niwayama au rachis) estimée chez 298 hommes âgés de 65 ans et plus, est de 42 %7.
Elle augmente considérablement avec l’âge chez ces hommes : 30 % pour 65-69 ans, 39 % pour 70-74 ans, 48 % pour 75-79 ans, 56 % pour 80 ans et plus. La prévalence de l’HVE peut être évaluée par scanner corps entier, comme dans l’étude japonaise publiée en 2018 et ayant porté sur 1479 patients âgé de 20 ans et plus, ayant eu un scanner dans le cadre d’un traumatisme8. La moyenne d’âge est de 54,7 ans et la prévalence de
l’HVE est de 19,5 % (critère de Resnick et Niwayama au rachis) : 21,1 % chez l’homme et 16 % chez la femme. La prévalence augmente avec l’âge : 16,5 % pour 50-59 ans, 28,7 % pour 60-69 ans, 40,9 % pour 70 ans et plus. L’HVE est possible mais assez rare avant l’âgede 45 ans.
La prévalence de l’HVE est corrélée avec l’âge, le sexe masculin, l’obésité (relation avec l’IMC démontrée dans 11 études), le syndrome métabolique, l’HTA, l’athérosclérose, le diabète (relation démontrée dans 7 études)5. Dans la cohorte prospective de Toronto de 938 patients atteints de rhumatisme psoriasique, une HVE radiographique (critères de Resnick et Miwayama au rachis thoracique) était présente chez 8,3 % des patients9. Les patients avec une HVE étaient plus âgés (63 vs 49 ans), avaient un IMC plus élevé, une uricémie plus élevée et avaient plus fréquemment un diabète et une HTA.
Description radiologique de l’hyperostose vertébrale engainante
Les ossifications de l’HVE sont souvent appelées ostéophytes ce qui est impropre puisque les ostéophytes font partie de la maladie articulaire qu’est l’arthrose et que l’HVE n’est pas une maladie articulaire mais bien une enthésopathie systémique. En pratique, la distinction n’est pas toujours facile, de même que la distinction entre les ossifications de l’HVE et les syndesmophytes de la spondylarthrite ankylosante (SPA). Chaque auteur
apporte une touche descriptive qu’il n’est pas forcément facile à voir et un élément comme le lieu de naissance des ossifications selon le mécanisme (ostéophyte d’arthrose, ossifications de l’HVE, syndesmophyte de la SPA), notamment par rapport à l’angle entre le corps et le plateau vertébral, est parfois impossible à déterminer et pas forcément discriminant. Certes, l’ossification de l’HVE est épaisse (contrairement au syndesmophyte), mais sa direction horizontale ou verticale est variable : moins verticale que le syndesmophyte, plus verticale que l’ostéophyte puisqu’elle évolue vers la formation d’un pont entre deux vertèbres. L’aspect en coulée prévertébrale (bien visible sur le profil) n’est pas spécifique puisqu’elle s’observe dans la SPA, mais ici la coulée est plus épaisse. L’aspect en coulée très hypertrophique est caractéristique au rachis cervical. Mais des ossifications de type HVE ont été décrites dans la SPA et inversement, les deux aspects pouvant coexister chez un même patient10.
Le rachis thoracique est le segment le plus touché dans l’HVE et particulièrement aux étages allant de T7 à T1110. Sur les clichés de face, la plupart des ossifications se situent sur le côté droit (face antérolatérale droite) et chez les patients ayant un situ inversus, elles sont visibles du
côté gauche, ce qui confirme l’hypothèse selon laquelle la présence de l’aorte, probablement par l’intermédiaire de ses battements, inhibe le développement des ossifications vertébrales dans l’HVE10. Ce rôle inhibiteur de l’aorte a aussi été mis en évidence, mais à un moindre degré, dans
la SPA dans une étude par scanner des syndesmophytes11. Des études longitudinales réalisées par scanner ont montré que les ossifications vertébrales progressaient de manière régulière avec le temps et que les ossifications naissant de deux vertèbres adjacentes se rejoignaient pour
fusionner et former le pont intervertébral10.
Les ossifications vertébrales lombaires de l’HVE sont présentes chez 30 % des patients ayant une atteinte du rachis thoracique10. L’atteinte du rachis cervical est présente chez environ un tiers des patients ayant une HVE10. Les ossifications cervicales de l’HVE sont souvent impressionnantes car hypertrophiques et formant des images en flammes de bougie ou en bec de perroquet. Contrairement au rachis thoracique, les ponts intervertébraux antérieurs sont symétriques par rapport à la ligne médiane10. Les ossifications peuvent être présentes de C2 à C7 (exceptionnellement C1) et sont les plus fréquentes de C3 à C6. Les très volumineuses ossifications peuvent entrainer des phénomènes de compression antérieure notamment de l’oesophage. L’atteinte cervicale de l’HVE peut être associée à une ossification du ligament longitudinal postérieur (OLLP), cette association étant présente dans 12 % des cas de la revue de la littérature12. Cette association n’est pas fortuite ce qui peut être expliqué pour partie par la prédominance chez l’homme âgé dans les deux pathologies et par l’association avec la diminution de la tolérance au glucose10.
Les ossifications périphériques de l’HVE siègent au niveau des enthèses et peuvent toucher les épaules, les coudes, les poignets, le pelvis, les hanches, les genoux, les chevilles. De manière caractéristique, elles sont volumineuses, épaisses, avec des ossifications des enthèses extra-articulaires comme la tubérosité tibiale antérieure l’olécrâne, les tendons d’Achille.
Les patients ayant une HVE peuvent avoir sur la radiographie du bassin un faux aspect d’ankylose sacro-iliaque faisant évoquer une SPA. L’utilisation du scanner des sacro-iliaques (SI) montre la fréquence des anomalies des SI dans l’HVE comme le démontre parfaitement le travail
israélien réalisé par l’équipe d’Eshed, publié en 201713. Ces auteurs ont comparé les scanners des SI de 104 patients ayant une HVE (critère de Resnick et Niwayama au rachis) et 106 sujets contrôles (pas de signe d’HVE) appariés pour l’âge et le sexe. L’âge moyen était de 72 ans (extrêmes 50-94) avec un sexe ratio hommes/femmes de 2,4. Les anomalies significativement plus fréquentes dans l’HVE par rapport à la population contrôle sont présentées au tableau 1. Les anomalies des SI que l’on trouve fréquemment dans l’HVE sont des ponts osseux formés par des ossifications des enthèses antérieures et postérieures, ou de la partie ligamentaire postérieure de la SI :
Tableau 1. Anomalies au scanner des sacro-iliaques dont la fréquence est significativement plus élevée dans une population de patients ayant une hyperostose vertébrale engainante en comparaison avec une population contrôle13.
| HVE | Contrôles | Odds ratio | Sensibilité (%) | Spécificité (%) | Valeur prédictive positive (%) | |
| Pont antérieur | 48% | 9% | 9.1 | 48.5% | 90.6% | 83.3% |
| Pont postérieur | 20% | 1% | 26.9 | 20.4% | 99.1% | 95.5% |
| Ankylose sacro-iliaque | 23% | 0% | 31.9 | 23.3% | 99.1% | 96% |
| Pont enthésophytique | 34% | 4% | 13.1% | 34% | 96.2% | 89.7% |
• pont osseux ostéophytique antérieur (situé en avant de l’articulation SI), avec une sensibilité de 48,5 % et une valeur prédictive positive (VPP) de 83 % ;
• pont osseux ostéophytique postérieur (situé en arrière de l’articulation SI) avec une sensibilité de 20 % et une VPP de 95 % ;
• pont enthésitique qui désigne un pont osseux entre os iliaque et os sacré, situé à la partie postérieure de la SI par ossification de la partie ligamentaire de la SI. Sensibilité 34 %, VPP 90 % ;
• aspect d’ankylose de la SI : sensibilité 23 %, VPP 96 %.
Des érosions des berges SI ne sont observées que chez 4 % des patients atteints d’HVE. Il n’y a pas de différence entre HVE et population contrôle pour les ostéophytes antérieurs ou postérieurs sans pont, pour la condensation sous-chondrale ou les géodes sous-chondrales.
L’intérêt du scanner des sacro-iliaques nous apparaît majeur dans les cas difficiles où le diagnostic hésite entre HVE et spondylarthropathie axiale, car les anomalies sont très différentes.
Aspects cliniques de l’hyperostose vertébrale engainante
Le fait de savoir si l’HVE entraîne une symptomatologie douloureuse spécifique est discuté.
Dans une étude réalisée en Suisse et publiée en 198914, en comparant 106 patients (moyenne d’âge 71 ans) ayant une HVE radiographique et 178 sujets n’ayant pas d’HVE radiographique (moyenne d’âge 68 ans), il n’a pas été retrouvé (par un questionnaire au patient) de différence de prévalence des rachialgies au cours des 6 mois précédents, ou auparavant, et ceci quel que soit l’étage (dorsal, cervical, lombaire).
Une vaste étude prospective réalisée à l’hôpital général de Montréal et publiée en 1997 dans la revue Medicine15, a comparé la fréquence des symptômes (douleurs et raideur) dans 3 populations : 56 patients ayant une HVE radiographique (âge moyen 67 ans), 43 patients ayant des lombalgies chroniques avec un spondylolisthésis lombaire (SDL) (âge moyen 63 ans) et 31 sujets contrôles (âge moyen 64,5 ans). Les symptômes au rachis dorsal étaient présents chez 43 % des patients ayant une HVE et 33 % des patients ayant un SDL. Les symptômes au rachis cervical étaient présents chez 61 % des patients avec une HVE et 58 % de ceux avec un SDL. On notait une fréquence plus élevée des douleurs périphériques chez les patients ayant une HVE. En termes d’échelle visuelle analogique, l’évaluation de la douleur à chaque étage rachidien était similaire entre patients ayant une HVE et ceux ayant un SDL. A l’examen physique, la raideur cervicale objective était plus importante dans l’HVE versus le SDL. Mais la mesure de la qualité de vie par le HAQ était similaire entre les 2 groupes de patients. Cette étude a comporté peu de patients et très peu de contrôles, mais elle montre qu’il n’y a pas de fréquence importante d’une symptomatologie douloureuse chez les patients ayant une HVE et non sélectionnés par une symptomatologie spécifique.
Dans l’étude réalisée aux USA et publiée en 2011, la fréquence des douleurs rachidiennes a été comparée entre 126 hommes ayant une HVE radiographique et 172 hommes n’ayant pas d’HVE radiographique7. Il a été fourni aux sujets de l’étude un questionnaire portant sur, d’une part les douleurs du rachis dorsolombaire et d’autre part celles du rachis cervical, ceci au cours des 12 derniers mois. Les hommes étaient tous âgés de 65 ans et plus. Les douleurs dorsolombaires étaient moins fréquentes chez les sujets ayant une HVE : 59 % vs 71 %. La fréquence des cervicalgies était similaire : 34 % vs 39 %. La qualité de vie, mesurée par le SF-12 était identique. Les auteurs émettent l’hypothèse que l’ankylose due aux ponts vertébraux diminue les rachialgies dorsolombaires chez ces patients âgés.
Ainsi, d’après ces 3 études, il n’apparait pas que l’HVE soit une cause fréquente de douleurs rachidiennes.
L’atteinte du rachis cervical de l’HVE peut entraîner une compression des structures aérodigestives situées en avant du rachis cervical, principalement une dysphagie par compression de l’oesophage et une obstruction des voies aériennes supérieures (VAES). Harlianto et coll. ont publié en 2022 une revue de la littérature sur 419 cas rapportés12. L’âge moyen était de 67 ans (extrêmes 35-91 ans) et le sexe ratio hommes/femmes était de 5,9/1. Une dysphagie était présente chez 414 patients et une obstruction des VAES chez 60 patients (55 patients avaient les deux types de symptômes). D’autres symptômes étaient parfois associés : cervicalgies postérieures (29 %), dysphonie (26 %), sensation de raideur cervicale (18 %). Plus rarement : syndrome d’apnée du sommeil, toux, insuffisance respiratoire, pneumopathie d’inhalation. La dyspnée était parfois sévère puisque certains patients ont nécessité une intubation ou une trachéotomie en urgence.
Les fractures rachidiennes de l’hyperostose vertébrale engainante
De manière générale, que ce soit dans l’HVE et dans la SPA, les fractures sont 4 fois plus fréquentes sur les rachis ankylosés par rapport aux rachis non ankylosés et il existe une augmentation du risque de compression médullaire dans ce type de fracture5. En effet, sur un rachis ankylosé, les contraintes mécaniques liées à la fracture ne peuvent pas se distribuer vers les zones mobiles comme les DIV, les articulations interapophysaires postérieures les ligaments, les capsules et les muscles paravertébraux. Donc ces forces sont plus importantes sur les structures osseuses. Typiquement, dans l’HVE, le trait de fracture passe dans le corps vertébral car l’os cortical des ossifications ponte totalement le DIV ce qui rend la partie médiane du corps vertébral moins résistante. Ces fractures vertébrales sont plus instables. Un diagnostic précoce est nécessaire pour éviter une aggravation, source de lésions de la moelle épinière. Dans 19 à 41 % des cas, il y avait un retard au diagnostic de fracture et chez ces patients
il y avait une atteinte neurologique dans 81 % des cas (versus 5 % en l’absence de retard diagnostique). Le retard diagnostique est en partie expliqué par le caractère souvent peu sévère du traumatisme chez un patient dont les rachialgies chroniques peuvent ne s’aggraver que modérément. La fracture peut être mal visible sur des radiographies standards et la suspicion diagnostique doit faire pratiquer un scanner et/ou une IRM. Il est intéressant de noter que la densité minérale osseuse mesurée par scanner n’est pas diminuée dans l’HVE3.
Physiopathologie de l’hyperostose vertébrale engainante
L’HVE est considéré comme une maladie dégénérative au cours de laquelle le ligament longitudinal antérieur et les enthèses s’ossifient progressivement9. La principale caractéristique de l’HVE est une néoformation osseuse en continuité avec la partie haute et la partie basse des
vertèbres et qui contient principalement de l’os cortical et à un moindre degré de l’os spongieux5. Le nouvel os se forme principalement au niveau des enthèses et il pourrait y avoir un rôle de différentes cellules ou tissus : fibroblastes, chondrocytes, fibres de collagène, matrice osseuse calcifié.
Il existe très peu d’études sur le caractère familial éventuel de l’HVE, même si 12 familles avec HVE et/ou chondrocalcinoses articulaires ont été décrites aux Açores16. L’HVE n’est pas associée à un allèle du système HLA. Les études ayant recherché une association avec des gènes du collagène sont négatives. Une étude asiatique a rapporté une association entre HVE et deux polymorphismes du gène FGF2. Au total, il n’existe pas de preuve d’un terrain génétique de l’HVE16.
Certains auteurs ont fait état d’un possible rôle de l’inflammation dans l’HVE. L’étude rapportée par Weiss et al.17 en 2016, compare l’IRM corps entier de 15 patients (âge moyen 66 ans) ayant une HVE symptomatique et de 33 patients (âge moyen 53 ans) ayant une SPA. Les résultats de cette étude (où les IRM n’ont été lues que par un seul lecteur) sont particulièrement difficiles à interpréter. Des anomalies inflammatoires et graisseuses sont mises en évidence au rachis et aux SI dans l’HVE, mais de manière beaucoup moins fréquente que dans la SPA.
L’équipe du service de rhumatologie de l’hôpital Cochin de Paris a mené une étude dont le but était très intéressant : il s’agissait d’étudier les anomalies IRM du rachis et des SI chez des patients atteints d’HVE18. Malheureusement la méthodologie de cette étude semble insuffisante, car sur les 53 patients sélectionnés de manière rétrospective le diagnostic d’HVE reposait sur le codage médico-administratif et seulement
41 patients avaient des radiographies disponibles du rachis et des SI. Dans cette série, 41 % avaient des lombalgies inflammatoires, 19,5 % avaient un aspect de sacro-iliite radiographique et 24 % des patients testés étaient porteurs du HLA-B27. La question de savoir si certains patients n’avaient pas une SPA (et non une HVE) était tranchée par l’avis d’un investigateur. Néanmoins, à la lecture des IRM du rachis, et sachant que la
prévalence des discopathies dégénératives était élevée chez ces patients d’âge moyen 65,6 ans, les anomalies étaient compatibles avec la définition de l’ASAS d’une spondyloarthrite (SpA) axiale chez 58 % des patients. À l’IRM des SI, seulement 16 % des patients avaient des anomalies compatibles avec une sacro-iliite inflammatoire de SpA axiale.
La maladie est favorisée par l’âge, le sexe masculin, le surpoids et le diabète. In fine, la physiopathologie de l’HVE reste à découvrir3,5. On pense qu’il existe d’une part un excès de facteurs de croissance (IGF1, TGF béta notamment) qui induit la transformation de cellules mésenchymateuses en ibroblastes et ostéoblastes ; et d’autre part, une réduction des peptides inhibant l’ostéoformation, comme la protéine matricielle Gla, la
BMP-2 et Dickkopf-13,10.
Association hyperostose vertébrale engainante et spondylarthrite ankylosante
D’assez nombreux cas d’association entre HVE et SPA ont été rapportés dans la littérature, comme celui rapporté par Ghossan en 202219 dont la réalité est indéniable puisque ce patient âgé de 57 ans s’était présenté avec une compression de l’oesophage et une paralysie de la corde vocale gauche secondaire à une ostéophytose exubérante cervicale d’HVE, alors qu’il présentait des rachialgies et des fessalgies depuis 4 ans, et que l’imagerie montrait une ankylose des articulations costovertébrales et costotransversaires (signe certain de SPA), ainsi qu’une sacroiliite inflammatoire à l’IRM. Chez ce patient HLA-B27 négatif, le scanner des SI montrait à la fois des ponts antérieurs typiques d’HVE et des érosions
des berges osseuses. D’ailleurs, chez ce patient un traitement par sécukinumab améliorait considérablement les douleurs et l’état fonctionnel.
Kuperus et coll.20 ont publié en 2018 une revue de la littérature des cas d’association entre HVE et SPA, n’en retenant que 39 cas (âge moyen 61 ans ; extrêmes 42-77), dont 90 % d’hommes. Seulement 33 % des patients testés étant porteur du HLA-B27. Si les anomalies radiographiques visibles au rachis étaient de type HVE et/ou SPA, les ossifications rachidiennes étaient en fait beaucoup plus souvent de type HVE. Le diagnostic de
SPA était souvent porté sur la radiographie du bassin, sachant qu’un scanner des SI n’était disponible que chez 28/39 de ces patients. Si l’association apparait certaine dans certains cas, d’autres n’étaient peut-être que des patients ayant une HVE.
|
CONCLUSION Nous n’avons que peu de certitude sur les manifestations cliniques douloureuses de l’HVE (nature, fréquence, évolution) et encore moins sur la physiopathologie de cette maladie. Pourtant, il semble que la majorité des rhumatologues s’accorde pour dire que, si l’HVE est le plus souvent une pathologie asymptomatique, il existe un pourcentage de patients présentant des douleurs ne trouvant pas d’autre explication que l’HVE. Il n’existe aucune recommandation thérapeutique particulière dans l’HVE, en dehors de celles données pour les complications compressives et fracturaires. Une meilleure connaissance de la maladie nécessiterait l’étude d’une cohorte de patients symptomatique présentant une HVE symptomatique, ou un état de pré-HVE (c’est-à-dire des ossifications vertébrales moins nombreuses que celles des critères de Resnick et Niwayama), dont il serait possible d’analyser les caractéristiques cliniques, biologiques, radiologiques (scanner, IRM), thérapeutiques, ainsi évidemment que l’évolution sur plusieurs années de suivi. Ceci n’est pas sans intérêt car les formes sévères existent ; nous nous souvenons d’une patiente que nous avions suivie pendant de très nombreuses années et pour laquelle toutes les tentatives thérapeutiques s’étaient avérées inefficaces, ne pouvant empêcher l’évolution vers un enraidissement complet du rachis cervical. |
RÉFÉRENCES
♦1. Forestier J, Rotes-Querol J. Senile ankylosing hyperostosis of the spine. Ann Rheum Dis 1950 : 9 : 321-30. ♦2. Kuperus JS, de Gendt EEA. Oner FC et al.
Classifi cation criteria for diffuse idiopathic skeletal hyperostosis: a lack of consensus. Rheumatology 2017 ; 56 : 1123-1134. ♦ 3. Mader R, Verlaan J-J, Eshed I et al.
Diffuse idiopathic skeletal hyperostosis (DISH): where we are now and where to go next. RMD Open 2017 ; 3 (1) : e000472. ♦4. Resnick D, Niwayama G. Radiographic and pathologic features of spinal involvement in diffuse idiopathic skeletal hyperostosis (DISH). Radiology 1976 ; 119 : 559-568. ♦5. Kuperus JS, Mohamed Hoesein FAA, de Jong PA, Verlaan JJ. Diffuse idiopathic skeletal hyperostosis: Etiology and clinical relevance. Best Pract Res Clin Rheumatol 2020 ; 34 : 101527.♦ 6. Westerveld LA, van Ufford HM, Verlaan JJ, Oner FC. The prevalence of diffuse idiopathic skeletal hyperostosis in an outpatient population in The Netherlands. J Rheumatol 2008 ; 35 : 1635-1638. ♦7. Holton KF, Denard PJ, Yoo JU, Kado DM, Barett-Conor E, Marshall LM. Diffuse idiopathic skeletal hyperostosis and its relation to back pain among older men: the MrOS Study. Semin Arthritis Rheum 2011 ; 41 : 131-8. ♦8. Hijama A, Katoh H, Sakai D, Sato M, Tanaka M, Watanabe M. Prevalence of diffuse idiopathic skeletal hyperostosis (DISH) assessed with whole-spine computed tomography in 1479 subjects. BMC Musculoskelet Disord 2018 ; 19 : 178. ♦9. Haddad A, Thavaneswaran A, Toloza S, Chandran V, Gladman DD. Diffuse idiopathic skeletal hyperostosis in psoriatic arthritis. J Rheumatol 2013 ; 40 : 1367-1373. ♦10. Eshed I. Imaging Characteristics of Diffuse Idiopathic Skeletal Hyperostosis: More Than Just Spinal Bony Bridges. Diagnostics (Basel) 2023 ; 13 : 563. ♦11. Tan S, Dasgupta A, Flynn JA, Ward %%. Aortic-vertebral interaction in ankylosing spondylitis: syndesmophyte development at the juxta-aortic vertebral rim. Ann Rheum Dis 2019 ; 78 : 922-928. ♦ 12. Harlianto NI, Kuperus JS, Mohamed Hoesein FAA et al. Diffuse idiopathic skeletal hyperostosis of the cervical spine causing dysphagia and airway obstruction: an updated systematic review. Spine J 2022 ; 22 : 1490-1503. ♦13. Leibushor N, Slonimsky E, Aharoni D, Lida M, Eshed I. CT Abnormalities in the Sacroiliac Joints of Patients With Diffuse Idiopathic Skeletal Hyperostosis. AJR Am J Roentgenol 2017 ; 208 : 834-7. ♦14. Schlapbach R, Beleyer C, Gerber NJ et al. Diffuse idiopathic skeletal hyperostosis (DISH) of the spine: a cause of back pain? A controlled study. Br J Rheumatol 1989 ; 28 : 299-303. ♦15. Mata S, Fortin PR, Fitzcharles M-A et al. A controlled study of diffuse idiopathic skeletal hyperostosis. Clinical features and functional status. Medicine (Baltimore) 1997 ; 76 : 104-117. ♦16. Couto AR, Paerreira B, Power DM et al. Evidence for a genetic contribution to the ossifi cation of spinal ligaments in Ossifi cation of Posterior Longitudinal Ligament and Diffuse idiopathic skeletal hyperostosis: A narrative review. Front Genet 2022 ; 13 : 987867. ♦17. Weiss BG, Bachmann LM, Pfi rrmann CW et al. Whole Body Magnetic Resonance Imaging Features in Diffuse Idiopathic Skeletal Hyperostosis in Conjunction with Clinical Variables to Whole Body MRI and Clinical Variables in Ankylosing Spondylitis. J Rheumatol 2016 ; 43 : 335-42. ♦18. Latourte A, Charlon S, Etcheto A et al. Imaging Findings Suggestive of Axial Spondyloarthritis in Diffuse Idiopathic Skeletal Hyperostosis. Arthritis Care Res 2017 ; 70 : 145-152. ♦19. Ghossan R, Zebouni SH, Farah TY, Fayad F. Diffuse Idiopathic Skeletal Hyperostosis and Ankylosing Spondylitis: A Challenging Case and Review of the Literature. J Radiol Case Rep 2022 ; 16 : 1-16. ♦20. Kuperus JS, Waalwijk
JF, Regan EA et al. Simultaneous occurrence of ankylosing spondylitis and diffuse idiopathic skeletal hyperostosis: a systematic review. Rheumatology 2018 ;
57 : 2120-2128.


